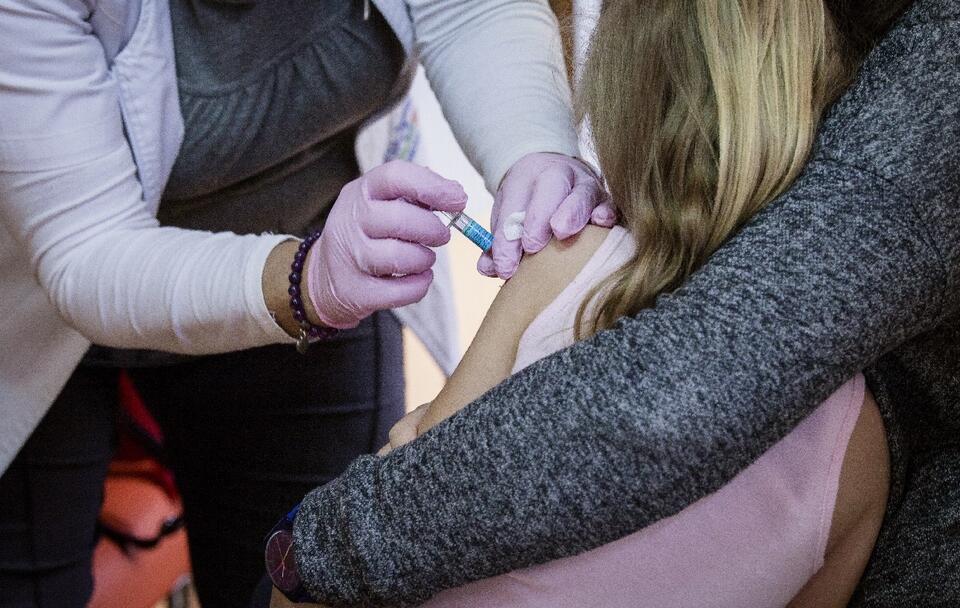Europejska Agencja Leków (EMA) zaleciła w czwartek zatwierdzenie szczepionki Comirnaty przeciwko Covid-19 dla dzieci w wieku od 5 do 11 lat. Badania kliniczne nad stosowaniem szczepionki przeciw COVID-19 u dzieci w wieku 5-11 lat były prowadzone także w Polsce – przypomniał w czwartek prezes urzędu rejestracji leków Grzegorz Cessak.
CZYTAJ WIĘCEJ: Szczepienia dzieci w wieku 5-11 lat już niedługo! Rzecznik MZ: „Pierwszych dawek szczepionki spodziewamy się w grudniu”
Szczepionka Comirnaty dla dzieci. Jest pozytywne zalecenie EMA
Agencja uznała, że korzyści ze stosowania preparatu Comirnaty u dzieci w wieku od 5 do 11 lat przewyższają ryzyko, szczególnie w przypadku chorób zwiększających ryzyko ciężkiego Covid-19.
U dzieci w wieku od 5 do 11 lat dawka szczepionki Comirnaty, opracowanej przez BioNTech i Pfizer, będzie niższa (10 µg), niż stosowana u osób w wieku 12 lat i starszych (30 µg). Podobnie jak w starszej grupie wiekowej, podaje się ją w postaci dwóch wstrzyknięć w odstępie trzech tygodni.
Najczęstsze działania niepożądane u dzieci w wieku od 5 do 11 lat są podobne do tych u osób w wieku 12 lat i starszych; obejmują m.in. zmęczenie, ból głowy, zaczerwienienie i obrzęk w miejscu wstrzyknięcia, ból mięśni i dreszcze - informuje Agencja.
Skuteczność preparatu obliczono u prawie 2000 dzieci
Główne badanie u dzieci w wieku od 5 do 11 lat wykazało, że odpowiedź immunologiczna na produkt Comirnaty, podany w niższej dawce (10 µg) w tej grupie wiekowej, była porównywalna z odpowiedzią obserwowaną po podaniu wyższej dawki (30 µg) osobom starszym w wieku 16-25 lat (na podstawie poziomu przeciwciał przeciwko SARS-CoV-2)
— przekazała EMA.
Skuteczność preparatu Comirnaty obliczono u prawie 2000 dzieci w wieku od 5 do 11 lat, u których nie wystąpiły objawy wcześniejszego zakażenia. Dzieci te otrzymywały szczepionkę lub placebo (zastrzyk pozorowany). Spośród 1305 dzieci otrzymujących szczepionkę u trzech rozwinął się COVID-19 w porównaniu z 16 z 663 dzieci, które otrzymały placebo. Oznacza to, że w tym badaniu szczepionka była w 90,7 proc. skuteczna w zapobieganiu objawowemu COVID-19 (chociaż rzeczywisty wskaźnik mógł wynosić od 67,7 proc. do 98,3 proc.)
— podała agencja.
EMA prześle teraz swoje zalecenie do Komisji Europejskiej, która podejmie ostateczną decyzję.
Badania kliniczne były prowadzone także w Polsce
Cieszę się z rekomendacji EMA dot. szczepień w grupie 5-11 l. Wydając zgodę na podjęcie badań klinicznych w Polsce w tej grupie wiekowej, @URPLWMiPB ma w tym swój udział. Stosunek korzyści płynących ze szczepienia dominuje nad potencjalnym ryzykiem wystąpienia działań niepożądanych
— napisał na Twitterze prezes Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Grzegorz Cessak.
Zamieścił informację, że badania fazy I, II i III prowadzone były w 94 ośrodkach na świecie. W badaniu I fazy (dobór dawki) wzięło udział 48 dzieci. W badaniu fazy II i III wzięło udział 2268 dzieci – 1517 otrzymało szczepionkę, a 751 placebo – podał Cessak.
Dawka szczepionki wynosiła 10 mcg (mikrogramów), podawano ją dwukrotnie w odstępie 21 dni. Skuteczność szczepionki, jak podał Cessak, wyniosła 90,7 proc.
Szczepionka Comirnaty jest obecnie stosowana u dorosłych i dzieci w wieku od 12 lat.
kpc/PAP
Publikacja dostępna na stronie: https://wpolityce.pl/spoleczenstwo/575513-ema-zaleca-szczepionke-dla-dzieci-badania-takze-w-polsce
Dziękujemy za przeczytanie artykułu!
Najważniejsze teksty publicystyczne i analityczne w jednym miejscu! Dołącz do Premium+. Pamiętaj, możesz oglądać naszą telewizję na wPolsce24. Buduj z nami niezależne media na wesprzyj.wpolsce24.